今回は
元素記号②He ヘリウムについて
書いていきます。

そもそも元素とは概念・そもそも原子とは?
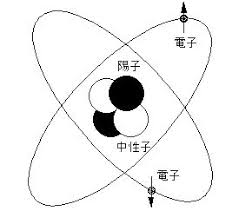
「原子」とは
中心である原子核とその
周囲を取り囲む電子によって構成されていて、
原子核は、さらに陽子と中性子から成り立っています。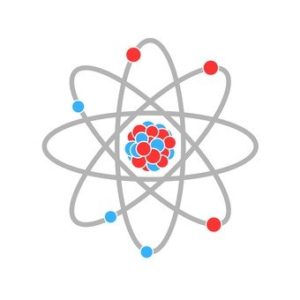
「元素」とは、概念であり
ざっくり簡単に書くと、どんな方法でも、
現在の科学で、これ以上分解することが出来ない・・
と、言える物質のことを言います。
その「原子」が含む「陽子」の数によって決定され
陽子の数が同じなら、同じ元素に分類されます。
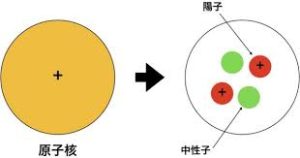
番号でそれを(陽子の数が同じ物)ナンバリングして、
分かりやすくした物が
「元素番号」となります。
ちなみに陽子の数(元素番号)は同じでも
陽子におくっついている、中性子の数が違う場合は
たとえば、水素・軽水素(1H )、重水素 (2H )と区別されます。

元素記号②He ヘリウム
ヘリウムとは希ガスに一種で、
化学変化がほとんど起きない、安定した元素と言われています。
宇宙では①H水素に次いで、2番目に多い元素となります。
無色、無臭、無味、無毒で
すべての元素の中で最も沸点が低く、加圧下でしか固体にならないそうです。
ヘリウムは地球の大気の 0.0005 % を占め、
鉱物などやミネラルウォーターの中にも溶け込んでいます。

ヘリウムは水素に次いで2番目に軽い気体で
水素と違い爆発の危険が無いことから
気球などにも使われています。
ヘリウムを発見したのは?
ヘリウムを発見したのは
イギリスの天文学者ノーマン・ロッキャー(1836~1920)となります。

1866年にインドで皆既日食を観察中
太陽光の中から新しいスペクトル線(一様で連続な光スペクトル上に現れる暗線または輝線)
ヘリウムを発見します
ヘリウムとはギリシャ語の「太陽」を示す言葉「ヘリオス」から
名付けられました。
ノーマン・ロッキャーは太陽の黒点の研究で有名で、
ヘリウムを発見した翌年には科学誌の
「ネイチャー」を創刊した人物です。

ヘリウムの用途
ヘリウムの用途で有名なのは
上記にも書きました気球での用途です
ヘリウムは水素の 92.64 % もの浮揚力があり、
燃えないため、水素よりも安全なガスとして気球または
風船等の浮揚用ガスとして利用されています。

ヘリウム中では音速が空気中よりずっと速いためヘリウムを
吸入してから発声すると、
あの甲高い音色の奇妙な声が出る事も有名ですね。

また工学では、
沸点、融点ともに最も低い元素であり、
液体ヘリウムは他の超低温物質よりも低温となるので
超伝導など、絶対零度に近い環境での
研究が必要な分野で冷媒として使用され、
また、人体に無害のため、医療などでも使用されています。
ヘリウムの同位体を紹介
「ヘリウム2」(ジプロトン)
ヘリウム2(ジプロトン)は、ヘリウムの仮想的な同位体で、
計算上は強い相互作用がもう2%大きかったら存在することができる。
「ヘリウム3」
陽子2個と中性子1個からなり、通常のヘリウム原子より軽い安定同位体、
地球大気中にはごく微量含まれるが、
地球生成時に地球深部のマントルに取り込まれたため、
地殻中よりもマントル中に多く存在する。
月面においては太陽風から供給されるヘリウム3が蓄積している。
重水素とヘリウム3との核融合は
そのクーロン障壁が高いため、核融合炉としての
実現が比較的容易とされています。

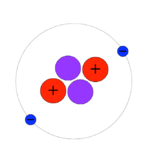
「ヘリウム4」
陽子2個と中性子2個からなり、
魔法数にあたり安定同位体である。
ビッグバン原子核合成によっても大量に生成された。
地殻岩石中の放射性元素の崩壊に伴うα粒子の蓄積によっても生成されるため、
地殻中に多く存在する。日本では100%輸入に頼っている。
「反ヘリウム」
反ヘリウムは、反陽子と反中性子からなる原子であり、
ヘリウムの反物質で記号はHeと、通常のHeに反物質であることを示す線を上に引く。
反ヘリウムの同素体の原子核として3Heと4Heがそれぞれ合成されている。
今のところ陽電子が周りを回る「反原子」と呼べる状態のものは合成されていない。
そのほか、人工的に作られた同位体としては、
ヘリウム6、ヘリウム8、ヘリウム10などがあります。
今回は以上です
有り難う御座いました